- Willkommen im Helios Klinikum Erfurt
Erfahrene Teams, moderne Medizintechnik, höchste pflegerische Standards: Unsere Abteilungen bieten optimale Bedingungen für Ihre professionelle medizinische Betreuung.
?qlt=85&ts=1738962911071&dpr=off)

?qlt=85&ts=1738962912296&dpr=off)

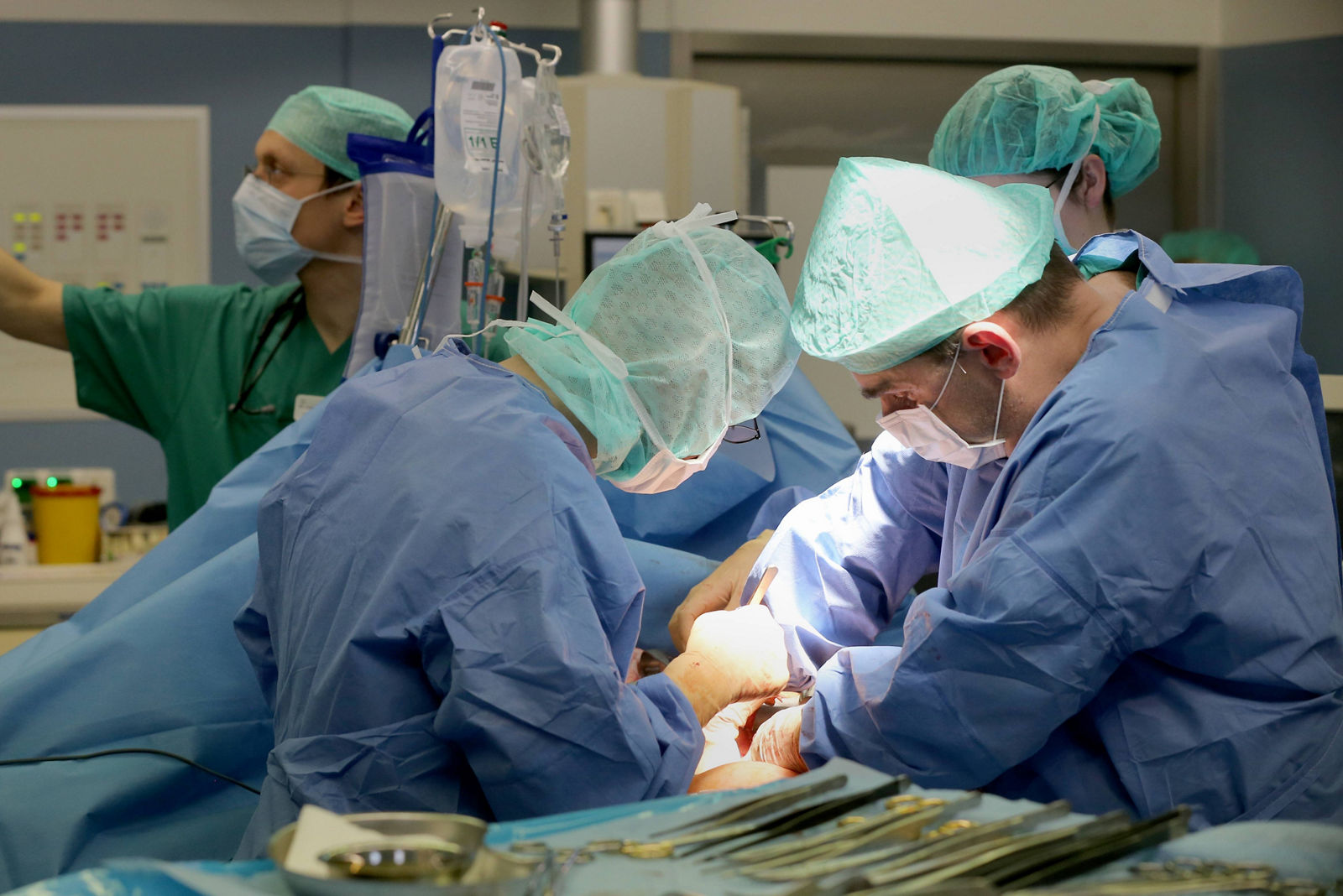
Das Lungenkrebszentrum des Helios Klinikums Erfurt setzt auf roboterassistierte Verfahren zur Abklärung und Therapie von Lungenkrebs.
Alper wollte als Anästhesietechnischer Assistent (ATA) arbeiten, egal, wie lang der Weg dorthin dauert. Als er nach Erfurt zog, gab es in Thüringen noch keine Blaupause für die Anerkennung ausländischer ATA-Abschlüsse. Er hat sie trotzdem als Erster durchgezogen und arbeitet heute im Anästhesie-Team des Helios Klinikums Erfurt.
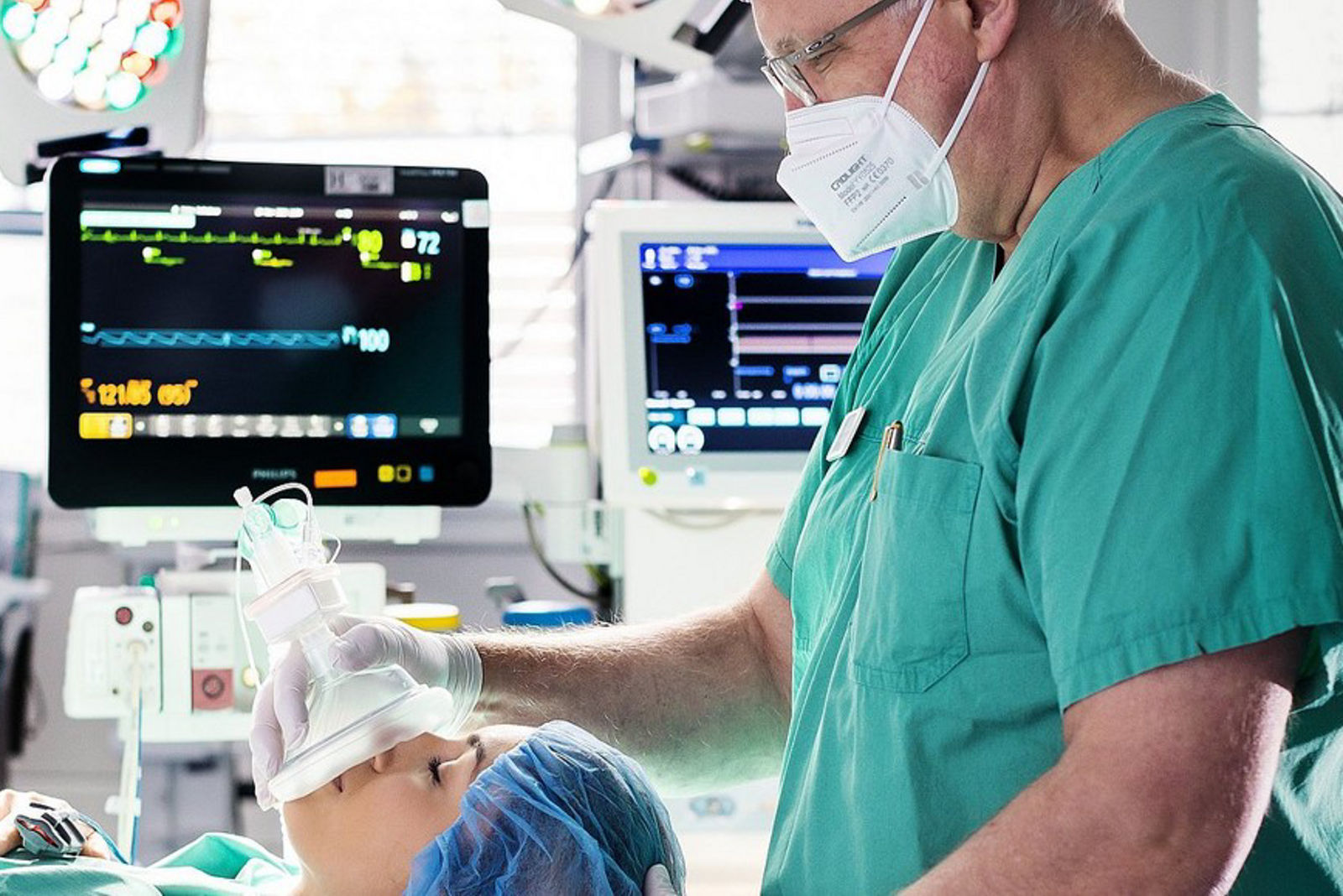
Narkosegase sind unverzichtbar für eine sichere Anästhesie. Zugleich zählen sie zu den größten direkten Emissionsquellen im Krankenhaus. Im Rahmen seiner Klimastrategie führt Helios seit 2023 in seinen Kliniken schrittweise eine Technologie ein, mit der Narkosegase in Aktivkohlefiltern aufgefangen und dem Recycling zugeführt werden, anstatt sie in die Außenluft abzugeben. Ab Mitte 2026 wird Helios rund 600 Narkosegasgeräte in 36 Kliniken in ganz Deutschland mit dieser Technologie ausstatten. Diese Kliniken verursachten 2025 insgesamt 80 Prozent der CO2 Emissionen im Bereich Narkosegase.
Helios kann mit seiner medizinischen Qualität überzeugen. Die nun für 2025 veröffentlichten Qualitätszahlen zeigen: Patientinnen und Patienten erhalten bei Helios eine Versorgung auf höchstem Niveau.
Mit der Einführung des Unit-Dose-Systems wird die Medikamentengabe in den Helios Kliniken standardisiert und optimiert. Das moderne System trägt dazu bei, die Sicherheit für Patientinnen und Patienten weiter zu erhöhen und Abläufe im Klinikalltag zu verbessern.
Eine Krebsdiagnose verändert oft das Leben für Betroffene ebenso wie für Angehörige. Neben der medizinischen Behandlung muss die Erkrankung auch seelisch verarbeitet werden. Häufig entsteht dabei der Wunsch nach Gesprächen, Orientierung und persönlicher Begleitung. Genau hier setzt die neue Krebsberatungsstelle am Helios Klinikum Erfurt an.
Die Klinik für Nuklearmedizin im Helios Klinikum Erfurt steht unter neuer Leitung: Priv.-Doz. Dr. med. Thomas Winkens hat die Position des Chefarztes übernommen. Er folgt auf Dr. med. Elke Conrad, die nach mehr als 35 Jahren engagierter, verantwortungsvoller und wegweisender Tätigkeit als Chefärztin in den wohlverdienten Ruhestand verabschiedet wurde.
Im Rahmen eines erstmalig durchgeführten, umfassenden Audits, bei dem Strukturen, Abläufe und Qualitätsstandards detailliert geprüft wurden, hat die Palliativstation des Helios Klinikums Erfurt das Zertifikat der ClarZert GmbH erhalten.
Neujahrsbaby 2026 im Helios Klinikum Erfurt: Yared Habte startet als erstes Kind ins neue Jahr

?qlt=85&ts=1744816222748&dpr=off)









:3-2)
:3-2)






