Prognose bei Lungenkrebs
Wird Lungenkrebs (auch Lungenkarzinom oder Bronchialkarzinom) in einem frühen Stadium festgestellt, kann er häufig vollständig entfernt oder so behandelt werden, dass eine langfristige Tumorkontrolle möglich ist.
Auch in fortgeschrittenen Stadien gibt es heute unterschiedliche Behandlungsoptionen, die das Leben verlängern und die Lebensqualität verbessern können. Zum Beispiel durch Immuntherapien oder zielgerichtete Medikamente.
Die Prognose, sprich die ärztliche Einschätzung, wie sich der Lungenkrebs voraussichtlich entwickeln wird, ist dabei nicht nur für die Betroffenen wichtig. Sie spielt zudem eine Rolle für die Wahl der Behandlungsmethoden.
Zu den Prognosefaktoren zählen:
- TNM-Klassifizierung und Stadium: Wie groß ist der Tumor, sind Lymphknoten befallen, gibt es Tochtergeschwülste?
- Histologie und Genotyp der Krebszellen: Wie sehen die Zellen unter dem Mikroskop aus? Liegen genetische Veränderungen vor?
Resektionsrandstatus (kurz R-Status): Wurde der Tumor durch eine Operation vollständig entfernt, oder verbleibt ein Tumorrest im Körper? - Das Geschlecht der Betroffenen: Frauen haben statistisch gesehen einen leichten Überlebensvorteil gegenüber Männern.
- Der Allgemeinzustand der Erkrankten: Wie belastbar ist die Patientin beziehungsweise der Patient? Welche Vor- oder Begleiterkrankungen gibt es?
Wichtig: Eine Prognose ist kein genauer Blick in die Zukunft, sondern eine Schätzung auf Basis von Erfahrungen, Studien und der persönlichen Situation jeder einzelnen Patientin und jedes einzelnen Patienten.

Lungenkrebsscreening: Bei dir wurde etwas entdeckt?
Ein auffälliger Befund ist noch keine Diagnose. Wir klären ab, was wirklich dahintersteckt – mit moderner Diagnostik und klarer Einordnung.
TNM-Klassifizierung und Stadium
Die TNM-Klassifizierung wird genutzt, um den Tumor einzuordnen:
- Das T steht hierbei für den Tumor und dessen Größe.
- N gibt Auskunft darüber, ob und wie viele Lymphknoten befallen sind („N“ für lateinisch „nodi“: der Knoten).
- Das M steht für Metastase und gibt an, ob und in welchem Umfang der Tumor gestreut hat.
Die Klassifizierung ist wichtig für die Stadieneinteilung. Bei Lungenkrebs werden grob vier Stadien unterschieden (I, II, III, IV), wobei jedes Stadium nochmals in weitere Untergruppen unterteilt werden kann.
Wichtig zu wissen: Die folgenden Zahlen sind Orientierungswerte aus großen Registerstudien. Sie beschreiben, wie viele Menschen fünf Jahre nach Diagnose noch leben – im Vergleich zu Personen ohne Lungenkrebs. Sie machen aber keine Aussage darüber, wie sich eine einzelne Erkrankung entwickelt. Die meisten verfügbaren Daten stammen zudem aus Erhebungen, die bereits einige Jahre zurückliegen. Die heute verfügbaren modernen Immuntherapien und zielgerichteten Therapien können die Prognose bei vielen Patienten relevant verbessern.
Das 5-Jahres-Überleben für nicht-kleinzelligen Lungenkrebs (NSCLC) in den Stadien I und II liegt ungefähr bei:
- Stadium IA: 80–93 Prozent
- Stadium IB: 73 Prozent
- Stadium IIA: 60–65 Prozent
- Stadium IIB: 53–55 Prozent
In den weiter fortgeschrittenen Stadien ist eine vollständige Heilung selten möglich. Moderne Therapien können die Erkrankung jedoch bei vielen Betroffenen über längere Zeit bremsen und Lebensqualität erhalten.
Beim selteneren kleinzelligen Lungenkrebs (SCLC) ist die Einteilung eine andere. Hier unterscheidet man in VLD, LD und ED:
VLD: Diese Abkürzung steht für „Very Limited Disease“ und bezeichnet ein Stadium, in dem die Ausbreitung der Erkrankung stark begrenzt ist. Die 5-Jahres-Überlebensrate liegt hier zwischen 35 und 70 Prozent.
LD: Diese Abkürzung steht für „Limited Disease“ und umfasst das Stadium, in dem die Ausbreitung der Erkrankung immer noch begrenzt ist.
ED: Die Buchstaben stehen für „Extensive Disease“ und meinen ein Stadium, in dem das kleinzellige Lungenkarzinom bereits weit fortgeschritten ist. Sobald der Tumor Metastasen gebildet und in andere Organe gestreut hat, wird die Erkrankung dieser Kategorie zugeordnet.
Aufgrund des relativ schnellen Wachstums und Streuung von kleinzelligen Lungenkarzinomen ist eine operative Behandlung nur noch selten möglich. Im Vordergrund stehen daher medikamentöse Behandlungen wir Chemotherapien und zunehmend auch Immuntherapien. Sie zielen darauf ab, das Tumorwachstum zu bremsen, Symptome zu lindern und die Lebenszeit zu verlängern.
Histologie und Genotyp der Krebszellen
Das Wort Histologie stammt aus dem Griechischen und bedeutet „Gewebelehre“. Im Zusammenhang mit Krebs bedeutet das: Pathologinnen und Pathologen untersuchen eine kleine eingefärbte Gewebeprobe unter dem Mikroskop, um genau zu bestimmen, um welche Art von Zellen es sich handelt und wie diese verändert sind.
Die Histologie gibt also Aufschluss darüber, wie sich der Krebs verhält, welche Therapien möglich und wie gut die Heilungschancen sind.
Lungenkrebs kann verschiedenen histologischen Typen zugeordnet werden. Die zwei Hauptgruppen sind:
- nicht-kleinzelliger Lungenkrebs (NSCLC): betrifft rund 80 bis 90 Prozent aller Lungenkrebsfälle
- kleinzelliger Lungenkrebs (SCLC): Betrifft rund 10 bis 15 Prozent aller Lungenkrebsfälle
Schon diese grobe Einordnung gibt einen Hinweis darauf, ob eine langfristige Heilung oder Tumorkontrolle möglich ist. Nicht-kleinzelliger Lungenkrebs wächst oft langsamer und kann häufiger operiert werden, wodurch er meist eine bessere Prognose hat.
Innerhalb der nicht-kleinzelligen Tumore unterscheidet man in weitere Untergruppen, von denen das Adenokarzinom und das Plattenepithelkarzinom die häufigsten sind.
Insbesondere Zellen des Adenokarzinoms tragen oftmals bestimmte genetische Veränderungen, sogenannte Treibermutationen. An diesen können zielgerichtete Medikamente angreifen und dadurch das Überleben der Patientinnen und Patienten in vielen Fällen deutlich verbessern.
Beim Plattenepithelkarzinom gibt es weniger solcher Mutationen und zielgerichteten Therapien, weshalb Chemo- und Immuntherapie weiterhin die Hauptrolle spielen.
Der Resektionsrandstatus (R-Klassifikation)
Der Resektionsrandstatus gibt an, ob der Krebs bei einer Operation komplett entfernt werden konnte oder ob am Schnittrand noch Krebszellen erhalten geblieben sind. Der Begriff R-Klassifikation geht zurück auf das englische „residual tumor“, das als „verbliebener Tumor“ übersetzt werden kann.
Die R-Klassifikation gibt also das Fehlen oder Vorhandensein eines Resttumors an. Man unterscheidet in:
- RX – ob ein Residualtumor vorhanden ist, kann nicht beurteilt werden
- R0 – kein Residualtumor: der Schnittrand ist frei von Krebszellen
- R1 – mikroskopischer Residualtumor: im Schnittrand sind Krebszellen verblieben, die unter dem Mikroskop sichtbar sind
- R2 – makroskopischer Residualtumor: Im Schnittrand sind Krebszellen verblieben, die mit den bloßen Augen sichtbar sind
Webinar Lungenkrebsscreening am 23. April 2026
Wie funktioniert das Screening? Ist es für dich sinnvoll? In unserem kostenfreien Webinar erklärt Lungenspezialist Prof. Dr. med. Tim O. Hirche, was du darüber wissen solltest – vom Ablauf des Screenings bis hin zur Frage, was nach einem positiven Befund passiert.
Bedeutung der Früherkennung für die Heilungschancen
Lungenkrebs wird bis heute meist erst in fortgeschrittenen Stadien erkannt, oft wenn der Tumor bereits gestreut hat. Statistisch befinden sich in Deutschland über 70 Prozent der Lungenkrebserkrankungen bei Erstdiagnose bereits in den prognostisch ungünstigen fortgeschrittenen Stadien III und IV.
Ziel der zukünftigen Diagnostik muss es daher sein, Tumoren bereits in früheren Stadien zu entdecken und ein sogenanntes „Stage-Shifting“ zu ermöglichen. Hierfür sind strukturierte Früherkennungsprogramme (Screenings) geeignet, in denen Risikogruppen wie starke oder ehemalige Raucherinnen und Raucher regelmäßig mit einer Niedrigdosis-Computertomographie (NDCT) untersucht werden. Inzwischen konnten zahlreiche internationale Studien zeigen, dass es auf diese Weise gelingt, Lungenkrebs in frühen Stadien zu diagnostizieren und die Sterblichkeit der Betroffenen zu senken.
Vor dem Hintergrund der wissenschaftlichen Erkenntnisse hat der gemeinsame Bundesausschuss (G-BA) im Juni 2025 beschlossen, ein Programm zum Lungenkrebs-Screening in Deutschland voraussichtlich ab April 2026 als Kassenleistung für gesetzlich Krankenversicherte zu etablieren. Für starke aktive sowie ehemaligen Raucherinnen und Raucher zwischen dem 50. und 75. Lebensjahr wird es dann möglich sein, sich einmal jährlich mittels NDCT auf Lungenkrebs untersuchen zu lassen. In Deutschland wir die Zahl der anspruchsberechtigten Personen auf 3 bis 5 Millionen geschätzt.
„Für eine gute Prognose bei Lungenkrebs gilt nach wie vor: Je früher der Lungenkrebs entdeckt wird, umso besser sind die Heilungschancen“, sagt Prof. Dr. Tim Hirche, Direktor der Klinik für Pneumologie in den Helios Dr. Horst Schmidt Kliniken Wiesbaden. Lungenkrebsspezialistinnen und -spezialisten empfehlen daher der Risikogruppe von starken aktiven und ehemaligen Raucherinnen und Rauchern, die neue Möglichkeit zur Früherkennung wahrzunehmen.
Sicherung von Lungenkrebs in Frühstadien mittels Bronchoskopieroboter „ION“
Die Einführung von Lungenkrebs-Screenings wird dazu führen, dass die Zahl von Tumoren, welche in Frühstadien entdeckt werden, stark ansteigt. Frühe Tumoren entstehen häufig im äußeren Bereich (Peripherie) der Lungen und weisen nur einen geringen Durchmesser auf. Das erschwert eine Gewebeentnahme zur histologischen Sicherung:
- Die herkömmliche Lungenspiegelung (Bronchoskopie), bei der über die zentralen Atemwege vorgegangen wird, kann peripher gelegene Herde oft nicht erreichen.
- Eine Punktion von außen unter CT-Kontrolle kann helfen, stößt jedoch bei sehr kleinen Herden (<1,5 cm) an ihre Grenzen und birgt ein erhöhtes Risiko für Komplikationen (insbesondere den Eintritt von Luft in den Pleuraspalt, den sogenannten Pneumothorax, oder eine Blutung)
Ein neuartiger Ansatz ist die roboter-assistierte Bronchoskopie (RAB). Für den Einsatz wurde dazu kürzlich der Bronchoskopieroboter „ION“ zugelassen. „ION ermöglicht erstmals, selbst millimeterkleine, peripher gelegene Gewebeverdichtungen in der Lunge präzise zu erreichen und zu biopsieren. Die Probenqualität ist besonders hochwertig, bei gleichzeitig sehr niedriger Komplikationsrate“, sagt Prof. Dr. Hirche.
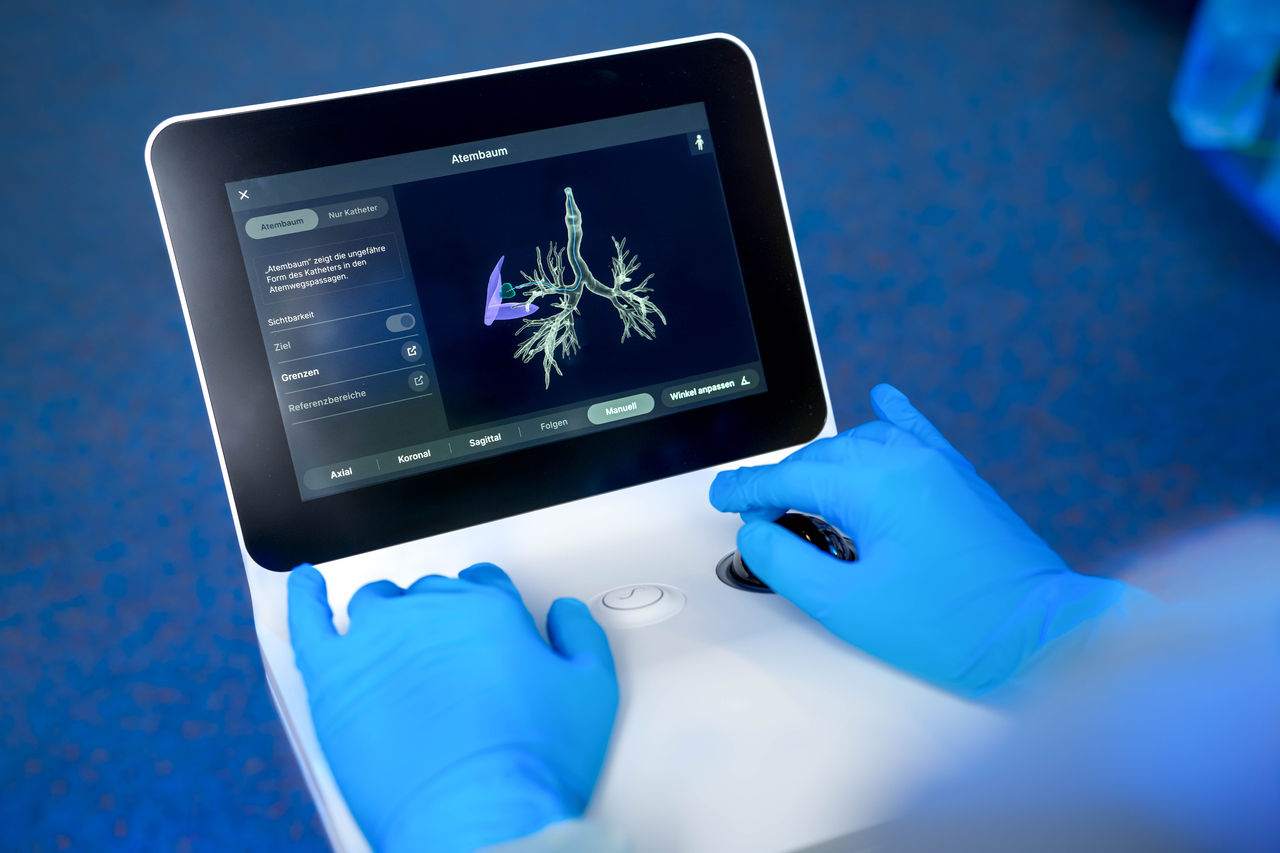
Funktionsweise von „ION“ – Schritt für Schritt:
- Planung vor dem Eingriff
Vor der Untersuchung wird ein hochauflösendes CT der Lunge angefertigt. Eine spezielle Software erstellt daraus ein dreidimensionales Modell der Atemwege, einen sogenannten „digitalen Zwilling“. Auf dieser Grundlage wird der optimale und sicherste Weg vom zentralen Atemweg bis zur verdächtigen Gewebeveränderung berechnet. - Einführen des Katheters
Während der Untersuchung wird ein ultradünner, flexibler Katheter mit integrierter Kamera und Positionssensoren über einen Beatmungsschlauch in die Bronchien eingeführt. Der Katheter ist mechanisch mit einem Roboterarm verbunden, der ihn stabil hält und präzise Bewegungen ermöglicht. - Steuerung durch den Arzt
Die Ärztin beziehungsweise der Arzt bedient über eine Steuerkonsole den Roboterarm, welcher die eigenen Bewegungen hochpräzise auf den Katheter überträgt. So kann der Katheter entlang des zuvor berechneten Pfades sicher bis in die peripheren, stark verzweigten Lungenabschnitte navigiert werden, millimetergenau und kontrolliert. - Gezielte Gewebeentnahme
Sobald der Zielherd erreicht ist, können die Ärztin oder der Arzt über den Katheter gezielt Biopsien entnehmen. Die genaue Position des Katheterendes wird dabei kontinuierlich in Echtzeit überwacht, sodass die Probenentnahme präzise und sicher erfolgen kann.
„Die robotisch-assistierte Bronchoskopie mit dem „ION“ System ist ein Paradigmenwechsel in der Lungenheilkunde. Wir können unseren Patientinnen und Patienten mit Verdacht auf ein Lungenkarzinom viel früher Gewissheit geben – und damit oft die Chance auf eine heilende Behandlung eröffnen“, sagt der Wiesbadener Lungenkrebsexperte.
FAQ
Lungenkrebs kann heilbar sein, wenn der Tumor sehr klein ist, nicht gestreut hat und komplett entfernt beziehungsweise zerstört werden kann. Vor allem die Stadien I und II bieten Chancen auf diesen Behandlungserfolg.
Mit „Prognose“ ist die ärztliche Einschätzung gemeint, wie sich eine Erkrankung voraussichtlich entwickeln wird. Dabei geht es unter anderem darum, wie hoch die Chancen auf Heilung sind, wie gut sich der Tumor kontrollieren lässt und welche Lebenserwartung möglich ist. Wichtig: Eine Prognose ist keine exakte Vorhersage. Auch Menschen mit gleicher Diagnose können sehr unterschiedliche Verläufe haben.
Die „5-Jahres-Überlebensrate“ beschreibt, wie viele von 100 Menschen mit einer bestimmten Krebsart und in einem bestimmten Stadium fünf Jahre nach Diagnose noch leben. Es ist eine statistische Größe für eine große Gruppe, keine Vorhersage für den einzelnen Menschen.
Sie gibt einen Eindruck wieder, wie gut eine Erkrankung im Durchschnitt behandelt werden kann, sagt aber nicht, ob Sie persönlich geheilt werden oder wie lange Sie leben werden.
Bei Lungenkrebs unterscheidet man grob in zwei Gruppen: nicht-kleinzelligen Lungenkrebs (NSCLC) und kleinzelligen Lungenkrebs (SCLC). NSCLC ist deutlich häufiger (ca. 80-85 Prozent aller Lungenkrebsfälle) und wächst meist etwas langsamer. Er kann in frühen Stadien öfter durch eine Operation vollständig entfernt werden und hat im Durchschnitt die bessere Prognose.
Wichtig: Die Prognose hängt nicht nur davon ab, ob der Tumor zur Gruppe NSCLC oder SCLC gehört. Es spielen noch viele weitere Faktoren eine Rolle:
- Das Stadium der Erkrankung
- Die molekularen Eigenschaften des Tumors (zum Beispiel bestimmte Genmutationen)
- Ihr Allgemeinzustand
- Wie gut die gewählte Therapie bei Ihnen persönlich wirkt
Eine Operation kann die Heilungschancen deutlich verbessern, vor allem wenn der Tumor lokal begrenzt ist und sich vollständig entfernen lässt. Dann besteht die Möglichkeit, langfristig tumorfrei zu bleiben.
Ja, es gibt heute Chancen auf Langzeitüberleben, auch wenn der Lungenkrebs bereits Metastasen gebildet hat. Durch neue Therapien, insbesondere Immuntherapien und zielgerichtete Medikamente, hat sich die Situation für einen Teil der Patientinnen und Patienten spürbar verbessert.
Trotzdem gilt: Metastasierter Lungenkrebs ist in den meisten Fällen keine heilbare Erkrankung im klassischen Sinn. Die Behandlung zielt eher darauf ab, das Tumorwachstum zu bremsen, Beschwerden zu lindern und die Lebenszeit zu verlängern.
Ja. Auch nach der Diagnose Lungenkrebs lohnt es sich, mit dem Rauchen aufzuhören. Studien zeigen, dass ein Rauchstopp die Prognose verbessern, das Risiko für einen weiteren Tumor senken und die Nebenwirkungen von Operation, Chemo- und Strahlentherapie verringern kann.
Wurde Ihr Tumor zufällig entdeckt, etwa im Rahmen einer anderen Untersuchung, haben Sie meist noch keine Beschwerden oder Symptome gespürt. Das macht es wahrscheinlicher, dass der Lungenkrebs in einem frühen und damit besser behandelbaren Stadium entdeckt wurde.
Lungenkarzinom, nicht-kleinzellig (NSCLC) — Onkopedia Online: https://www.onkopedia.com/... (Zugriff am 26.11.2025)
Krebs - Krebs in Deutschland Online: https://www.krebsdaten.de/... (Zugriff am 26.11.2025)