Sie können Ihren Termin entweder telefonisch oder ganz bequem über unser Patientenportal buchen.
Sekretariat Chirurgisches Zentrum
Telefon: 0202 896-2474
Fax: 0202 896-2930
Mo-Do 07:30-15:30 Uhr, Fr 07:00-13:30 Uhr
Notfallpatient:innen stellen sich bitte ohne Termin im interdisziplinären Notfallzentrum (NFZ) in Haus 5 EG vor.
Von der Vorsorge und modernen Diagnostik über minimalinvasive Operationen bis hin zu Chemotherapie, Strahlentherapie und strukturierter Nachsorge: Im Darmkrebszentrum Wuppertal bieten wir Ihnen die komplette Versorgung aus einer Hand – leitliniengerecht, zertifiziert und individuell auf Sie zugeschnitten.
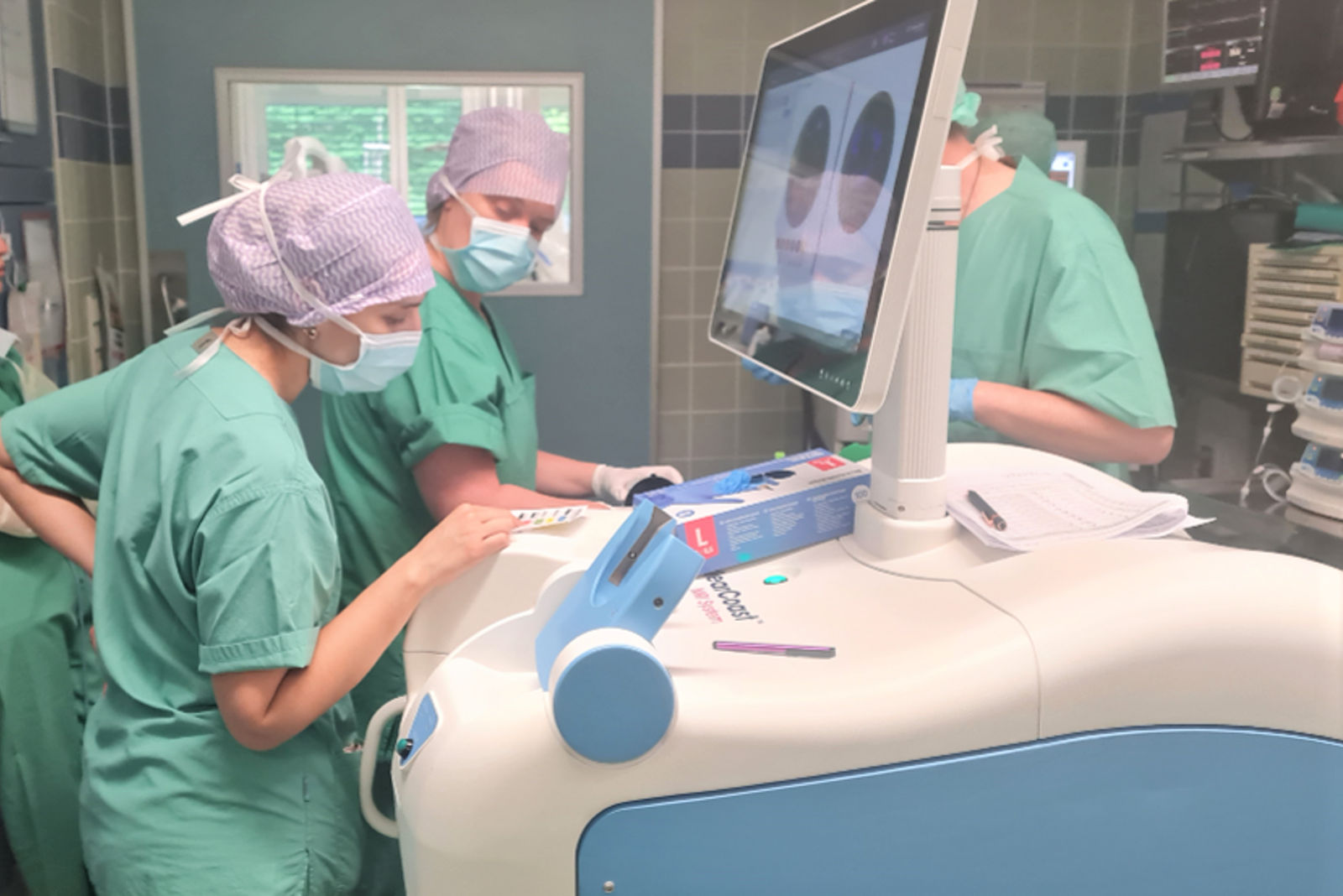
Für die genaue endoskopische Untersuchung des Darmes nutzen wir die neueste Generation von hochauflösenden Video-Koloskopen mit verschiedenen Lichtfiltern und Zoom-Funktion.
Dies erlaubt schon vor der mikroskopischen Aufarbeitung von entfernten Polypen und während der Endoskopie durch die Zuhilfenahme international gültiger Klassifikationssymsteme eine Zuordnung in gutartige oder bösartige Polypen, was das weitere therapeutische Verfahren entscheidet.
Therapie
Neben den gängigen Polypen-Abtragungen mit der Schlinge nach oder ohne Unterspritzung (sog. Polypektomie und endoskopische Mukosaresektion) bieten wir die endoskopische Vollwand-Resektion (EFTR) als endoskopisch-interventionelles Resektions-Verfahren an (z. B. bei Polypen in einem Darmdivertikel, Polypen am Appendix-Abgang oder Polypengewebe im Narbenbereich), bei dem der Darmpolyp mit dem tragenden Wand-Areal durch eine Stromschlinge ausgeschnitten und die Wand mit einer Klammer (sog. Clip) verschlossen wird. Zudem bieten wir die endoskopische Submukosa-Dissektion (ESD) zur Entfernung größerer und von der Beschaffenheit der Oberfläche auffälliger Darmpolypen an, bei dem das Risiko einer frühen bösartigen Veränderung besteht. Hierbei handelt es sich um eine endoskopische Abtragung von Polypen mit einem Strommesser unterhalb der Schleimhaut, sodass ein Polyp im Ganzen zur histologischen Begutachtung an den Pathologen gegeben werden kann.
Sowohl die ESD als auch die EFTR erlauben es, höhergradig veränderte Polypen, Rezidiv-Polypen im Narbengewebe und Darmkrebs im frühen Stadium vollständig endoskopisch zu behandeln, so dass ein weitergehender operativer Eingriff nicht erfolgen muss. Liegt Darmkrebs im frühen Stadium vor, so wird der Patient zuvor im interdisziplinären Tumorboard vorgestellt und die endoskopische Therapie gemeinsam entschieden.
Bei der Wahl der Operationsmethode ist es ausschlaggebend, ob Sie an einem Dickdarm- oder Enddarmkrebs erkrankt sind. Man spricht von Enddarmkrebs, wenn der Tumor bis 16cm oberhalb der Schleimhautfalte am After sitzt.
Die Operation bei Dickdarmtumoren
(Kolonkarzinome = bösartige Dickdarmtumore)
Unser Expertenteam beschließt in der interdisziplinären Tumorkonferenz, welches Therapiekonzept für Sie am besten geeignet ist. Dazu zählt neben einer eventuell notwendigen Chemotherapie oder Bestrahlung auch die Operation. In den letzten Jahrzehnten wurde für jede Tumorlokalisation, also jeden Punkt im Darm, an dem sich ein Tumor befinden kann, das jeweils beste Operationsverfahren im Rahmen wissenschaftlicher Studien festgelegt. Der Haupttumor und alle Lymphgefäße, Lymphknoten und Blutgefäße, durch die der Tumor in den Körper „streuen“ kann, werden bei allen Operationsmethoden aus dem Körper entfernt. Das Ausmaß der Darmentfernung wird durch Lagebeziehung zu den versorgenden Blut- und Lymphgefäßen und das hierdurch definierte Lymphabflussgebiet vorgegeben.
Bei diesen Operationen wird der Darm in der Regel wieder wie zwei Schlauchenden mit Handnähten oder automatischen Klammernahtgeräten wieder zusammengefügt. Selten muss bei Dickdarmtumoren ein künstlicher Darmausgang angelegt werden.
Die Operation bei Mastdarmturmoren
(Rectumkarzinome = bösartige Mastdarmtumore)
Die operative Therapie des bösartigen Mastdarmtumors erfordert in der Regel neben der Entfernung des tumortragenden Mastdarms auch die Entfernung des Fettgewebes mit Blutgefäßen, Lymphgefäßen und Lymphknoten um den Mastdarm (Mesorectum) und damit des regionären Lymphabflussgebiets. Die Besonderheit bei den Mastdarmtumoren ergibt sich durch die enge Lagebeziehung zum Schließmuskel, der eventuell entfernt werden muss, wenn der Tumor bis nah an den Muskel heranreicht.
Multiviszerale Chirurgie
(Entfernung von Darm und Nachbarorganen)
Wenn bösartige Darmtumore an Nachbarorganen festkleben oder in diese eingewachsen sind, müssen die Nachbarorgane mit entfernt werden, damit Sie geheilt werden können (multiviszerale Resektion). Wenn bei Ihnen ein solcher Fall vorliegt, wird Ihr Stationsarzt das Vorgehen im Einzelfall mit Ihnen ausführlich besprechen.
Im Rahmen von Erkrankungen des Darm-Traktes können Schmerzen auftreten. So ist es möglich, dass noch in der Zeit der Abklärung oder im Verlauf bei gut- oder bösartigen Tumoren manchmal das Symptom Schmerz im Vordergrund steht. Dann kann im Rahmen einer gezielten Schmerztherapie mit unterschiedlichsten Verfahren die Schmerzlinderung erreicht werden.
Während und nach der Operation
Bei Operationen können Schmerzen durch eine gezielte Schmerztherapie (u. a. mit Schmerztherapiekathetern) vorgebeugt und diese wirksam gelindert werden. Dabei arbeiten Pflegekräfte, Mitarbeiter des Akutschmerzdienstes, Operateure und Stationsärzte eng zusammen.
Wieder zu Hause
Auch nach dem stationären Aufenthalt wird die Weiterversorgung nahtlos fortgesetzt. Der Hausarzt wird über die aktuelle Schmerzmedikation informiert. Zusätzlich kann, wenn es erforderlich und gewünscht wird, die Weiterbetreuung bei einem Arzt für spezielle Schmerztherapie vermittelt werden.
Im Team gegen Schmerzen
Geleitet wird die Schmerztherapie von Frau Dr. Mielke, Oberärztin der Klinik für Anästhesiologie. Sie hat eine spezielle Weiterbildung in der Schmerztherapie absolviert. Zu ihrer Unterstützung und damit zur optimalen Versorgung der Patienten steht ein engagiertes Team an besonders geschulten Mitarbeitern zur Verfügung.
Unter Mitwirkung aller Beteiligten ist es so möglich, dass den Patienten, die an Schmerzen leiden, rasch und wirksam geholfen wird.
Bei Patienten mit bösartigen Tumoren des Rektums (Mastdarm), die die Darmwand überschreiten oder die die angrenzenden Lymphknoten im Beckenbereich befallen haben, ist neben der operativen Tumorentfernung die Strahlentherapie − ggfs. mit begleitender Chemotherapie − eine wichtige Säule der Therapie. Das Ziel ist die Heilung der Erkrankung.
Das Rektum (Mastdarm) ist ungefähr 16 cm lang (mit einem starren Endoskop von der sogenannten Anokutan-Linie gemessen, der Stelle, wo der Anus in die Gesäßhaut übergeht).
Man unterteilt das Rektum in
− das tiefsitzende Rektum (0−6 cm ab Anokutanlinie)
− das mittlere Rektum (6−12 cm a. A.) und
– das obere Rektum (12−16 cm a. A.)
Bei Tumoren des oberen Rektums wird eine Strahlentherapie zurückhaltend gesehen und die Therapie analog zu der des Dickdarmkrebses ausgerichtet.
Ob eine Strahlentherapie sinnvoll ist oder auch eine zusätzliche Chemotherapie indiziert ist, wird immer interdisziplinär in der gemeinsamen Konferenz unseres zertifizierten Darmkrebszentrums entschieden.
Ist eine Strahlentherapie aufgrund des Ausbreitungsstadiums sinnvoll, kann diese entweder vor oder nach der Operation durchgeführt werden. In den letzten Jahren hat sich aber gezeigt, dass eine präoperative (neoadjuvante) Strahlentherapie zu besseren Ergebnissen führt und auch deutlich besser vertragen wird. Daher wird dieses Vorgehen, wenn möglich, bevorzugt.
Manchmal kann aber die primäre Operation sinnvoll sein, z.B. bei Tumoren, die noch in einem früheren Stadium sind und eine zusätzliche Strahlentherapie nicht nötig ist, oder auch bei Tumoren, die durch Blutung oder Verschluss des Darmes Probleme machen.
Bei einer tumorbedingten Enge des Darmes kann es sinnvoll sein, vor Beginn einer neoadjuvanten Bestrahlung vorübergehend ein Stoma (künstlicher Darmausgang) anzulegen, damit die Darmpassage funktioniert. Sollte dies notwendig sein, werden Sie unsere Ärzte und unsere Stomaberatung ausführlich informieren.
Das Ziel der genannten Therapien ist eine dauerhafte Heilung.
Mögliche Arten der Bestrahlung vor einer Operation
Es gibt zwei verschiedene Therapieschemata der neoadjuvanten Bestrahlung, die je nach Situation und Ausbreitungsstadium eingesetzt werden:
1. KURZZEIT-VORBESTRAHLUNG
Diese Strahlentherapie erfolgt präoperativ und dauert eine Woche (5 Bestrahlungen). Sie erfolgt entsprechend an 5 Tagen innerhalb einer Woche mit höherer täglicher Dosis.
Die OP erfolgt dann rasch innerhalb von 3–5 Tagen nach Ende der Bestrahlung. Eine parallele Chemotherapie erfolgt bei der Kurzeit-Vorbestrahlung nicht.
2. RADIO-CHEMOTHERAPIE
Bei dieser Behandlung erhalten die Patienten eine Bestrahlungsserie über 5 ½ Wochen (25 bis 28 Bestrahlungen). Die Bestrahlung wird jeweils an fünf Tagen der Woche von Montag bis Freitag durchgeführt. Parallel dazu erfolgt eine Chemotherapie, meist in Tablettenform oder als Infusion.
Diese Behandlung wird gegenüber der Kurzzeit-Vorbestrahlung bevorzugt, wenn die Erkrankung schon weiter fortgeschritten ist und/oder eine Tumorverkleinerung (Schrumpfung) vor der OP erwünscht ist. Dies kann sinnvoll sein z.B. bei Tumoren, die nahe am Darmausgang liegen, um den Schließmuskel erhalten zu können (sogenannte „kontinenzerhaltende“ OP).
Die OP erfolgt dann etwa 6–8 Wochen nach Abschluss der kombinierten Behandlung.
Nach der Operation wird in einer erneuten gemeinsamen Konferenz geprüft, ob noch eine Fortsetzung der Chemotherapie notwendig ist. Dies ist von initialen und postoperativen Tumorstadium abhängig.
Neues Konzept „Organerhalt“
Aktuelle Studien geben Hinweise, dass unter bestimmten Voraussetzungen nach erfolgter Radiochemotherapie der Verzicht auf die Operation erwogen und der Enddarm somit komplett erhalten werden kann („Organerhalt“).
Die Datenlage ist aber noch zu begrenzt, um eine eindeutige Empfehlung abgeben zu können.
Daher ist ein solches Vorgehen eine individuelle Entscheidung, die unter Abwägung vieler Faktoren interdisziplinär und im Gespräch mit dem Patienten entschieden werden muss. In dem Gespräch mit dem Patienten müssen die Erwartungen und Wünsche des Patienten an die Therapie, an die onkologische Sicherheit und auch die Lebensqualität fokussiert werden.
Voraussetzungen für ein organerhaltendes Vorgehen sind u.a:
klinisch und in den Kontrolluntersuchungen vollständige Rückbildung des Tumors unter der Radiochemotherapie
lokal begrenztes Tumorstadium, keine befallenen Lymphknoten
engmaschige Nachsorge
Die genauen Voraussetzungen, aber auch möglichen Risiken einer organerhaltenden Therapie bei Rektum-Karzinom besprechen wir gerne mit Ihnen in einem persönlichen Gespräch.
Postoperative Radiochemotherapie
In seltenen Fällen kann es sein, dass anhand der präoperativen Untersuchungen von einem frühen Stadium der Erkrankung auszugehen ist, die feingewebliche Untersuchung des Pathologen postoperativ aber eine fortgeschrittenere Erkrankung ergibt. In diesem Fall wird die Operation zeitnah durchgeführt.
Sollte sich nach der mikroskopischen Untersuchung durch unsere Pathologen ein fortgeschritteneres Stadium zeigen (z.B. Wachstum über die Darmwand oder ein Tumorbefall der angrenzenden Lymphknoten), wird postoperativ eine kombinierte Strahlen- und Chemotherapie über 5 ½ Wochen in gleicher Weise wie präoperativ durchgeführt. An die fünfeinhalbwöchige Bestrahlungsserie mit begleitender Chemotherapie schließt sich dann in der Regel noch eine alleinige Chemotherapie an.
Im Mittelpunkt einer onkologischen strahlentherapeutischen Behandlung steht in unserem Haus der Mensch, der sich uns anvertraut. Denn eine isolierte Betrachtung der Tumorerkrankung wird unserer Auffassung nach der Gesamtsituation nicht gerecht. Dieser ganzheitliche Ansatz kann mit Hilfe der komplementären Medizin unterstützt werden.
Die Komplementärmedizin ist eine unterstützende Therapieform, die zusätzlich zur konventionellen „schulmedizinischen“ Behandlung, die die Basis darstellt, angewendet werden kann. Ziel der komplementärmedizinischen Behandlung ist es, Nebenwirkungen der konventionellen Tumortherapie zu vermindern, die Lebensqualität zu erhöhen sowie Stress und Belastungen, die im Zusammenhang mit der Erkrankung stehen, zu reduzieren.
Wenn Sie das wünschen, können wir – neben der notwendigen konventionellen onkologischen Therapie und insbesondere der Strahlentherapie – sinnvolle, unterstützende (komplementärmedizinische) Maßnahmen anbieten.
Falls Sie Fragen zu komplementärmedizinischen Aspekten oder besondere Wünsche haben, sprechen Sie uns gerne an.
Ein Bauchfellkarzinom ist eine häufige Metastase vieler Krebserkrankungen. Dank stetiger Weiterentwicklung der Medizin und fortschrittlicher Technik können heute manche Patienten mit Peritonealkarzinose durch eine Operation kombiniert mit einer intraoperativen Chemotherapie behandelt werden.
Die Peritonealkarzinose, der Befall des Bauchfells durch einen bösartigen Tumor, ist ein Zeichen von fortgeschrittener Tumorerkrankung. Lange galt dieser Zustand als inoperabel bzw. unheilbar. Die einzige Therapieoption stellte die palliative Chemotherapie dar.
Dank stetiger Weiterentwicklung der Medizin und fortschrittlicher Technik können heute manche Patienten mit Peritonealkarzinose durch eine Operation kombiniert mit einer intraoperativen Chemotherapie behandelt werden. Das Ziel ist hierbei die lokale Kontrolle des Tumors unter Erhaltung der Lebensqualität, wobei in einzelnen Fällen auch eine Heilung möglich ist.
In unserem Zentrum stellen wir jeden Patienten mit einem Tumorleiden im interdisziplinären Tumorboard vor, wo Experten aus den behandelnden Fachabteilungen (Chirurgie, Onkologie, Gastroenterologie, Strahlentherapie, Nuklearmedizin, Radiologie und Pathologie) die bestmögliche Therapie individuell festlegen und planen. Hiermit erreichen wir, dass Patienten identifiziert werden, die mit Peritonealkarzinose von einer chirurgischen Therapie profitieren können. Hierzu bieten wir alle gängigen Methoden in Form von HIPEC und PIPAC an.
HIPEC (hypertherme intraperitoneale Chemoperfusion)
Bei der HIPEC handelt es sich um ein Verfahren, wo eine ausgedehnte, oft multiviszerale, chirurgische Tumorentfernung und die partielle oder komplette Entfernung des Bauchfells mit der chemotherapeutischen „Spülung“ des Bauchraumes kombiniert werden.
Durch die chirurgische Therapie werden alle makroskopischen, also sichtbaren Tumorherde entfernt. Die anschließende lokale Chemotherapie dient dem Ziel, auch mikroskopisch kleine, nicht sichtbare Reste des Tumors abzutöten. Hierbei wird die Wirksamkeit der Chemotherapie durch die „vor Ort“ - Wirkung und durch Erhitzen der Chemotherapielösung auf ca. 42°C gesteigert.
Die HIPEC ist eine aufwändige und für den menschlichen Körper sehr belastende Methode, welche meistens nur einmal durchgeführt werden kann und leider nicht für jeden Patienten geeignet ist. Die Auswahl der Patienten muss sorgfältig erfolgen, damit nur diejenigen behandelt werden, die von den Vorteilen der Therapie trotz Nebenwirkungen tatsächlich profitieren.
PIPAC (pressurized intraperitoneal aerosol chemotherapy)
Die PIPAC ist eine innovative Methode zur Therapie der Peritonealkarzinose, die deutlich weniger belastend und dadurch besser verträglich ist, als die HIPEC. Hierbei wird im Rahmen einer Laparoskopie (Bauchspiegelung) eine lokale Tumortherapie mit einer Chemotherapielösung in Aerosolform durchgeführt. Der erhöhte Druck im Bauchraum sorgt für eine bessere Gewebezugänglichkeit der Chemotherapie.
Auch wenn die PIPAC keine Heilung erbringen kann, so kann durch diese schonende Technik oft eine deutliche Besserung der Lebensqualität und eine Verlängerung der Lebenszeit erreicht werden. Zudem ist diese Methode auch mehrfach durchführbar. Im Falle eines guten Ansprechens kann die positive Wirkung mehrmals ausgenutzt werden.
Das Institut für Pathologie und Molekularpathologie bedient das gesamte Spektrum moderner pathologischer, zytologischer und molekularpathologischer Methoden. Mit neuesten Untersuchungsverfahren und modernster technischer Ausstattung helfen wir für jeden Patienten im Rahmen einer personalisierten Krebsmedizin / Präzisionsonkologie, die passgenaue Therapie mit zielgerichteten Substanzen zu finden.
Somit können möglichst effektive Therapiemöglichkeiten identifiziert und gleichzeitig weniger wirksame und stärker belastende Therapien vermieden werden.
Die molekulare Charakterisierung des Tumorgewebes (Untersuchung des Erbguts der Tumorzellen) hat die diagnostischen und therapeutischen Möglichkeiten bei Tumorerkrankungen in den letzten Jahren wesentlich erweitert. Eine umfassende molekulargenetische Tumorcharakterisierung lässt ein tieferes Verständnis der molekularen Grundlagen eines Tumors zu, was eine individuelle, zielgerichtete Therapie für jeden einzelnen Patienten ermöglichen kann. Die Anzahl der genetischen Veränderungen variiert dabei von einigen wenigen bis zu vielen Hunderten in Abhängigkeit der Krebsform. Diese Veränderungen unterscheiden sich nicht nur zwischen den einzelnen Krebsformen, sondern variieren auch teilweise wesentlich von Patient zu Patient. Hierbei gilt es, die genetischen Veränderungen zu erkennen, die wesentlich für die Tumorentstehung des spezifischen Patienten sind. Diese Veränderungen stellen dann mögliche therapeutische Zielstrukturen dar, die durch ein oder mehrere Medikamente angegriffen werden können.
Neben der Sequenzierung großer Gen-Panels zur individuellen Tumoranalyse jedes Patienten mit soliden Tumoren steht im Institut für Pathologie und Molekularpathologie auch die Analyse genetischer Veränderungen des Tumorgewebes aus dem Blut (sogenannte „Liquid Biopsy“) zur Verfügung. Im Rahmen dieser Untersuchungen werden aus den Tumorproben zahlreiche krebsassoziierte Gene sequenziert, um klinisch relevante Veränderungen zu erkennen. Zusätzlich wird im Rahmen der Genexpressions-Diagnostik die Aktivität von verschiedenen Genen in den Krebszellen und damit auch das Risiko für ein Wiederauftreten des Tumors untersucht. Bei Patientinnen mit Brustkrebs kann ein Genexpressionstest sinnvoll sein, wenn die medizinischen Faktoren nicht eindeutig für oder gegen eine Chemotherapie sprechen. Darüber hinaus werden umfassende Untersuchungen von veränderten Eiweißmustern und Signalwegen in den Tumorzellen als diagnostisches Werkzeug durchgeführt. Die Ergebnisse werden dann im Rahmen einer Tumorkonferenz besprochen, um für jeden Patienten die bestmögliche Therapie zu finden.
Beim Operieren mit dem Da Vinci®-Operationssystem unterstützt ein Computer mit feinen Geräten die Handbewegungen des Operateurs ausgleichend und erweitert zudem erheblich seinen Aktionsradius.
Technik der neusten Generation
Computerassistiertes Operieren mit Da Vinci®
Mit extrem winzigen und wendige Instrumenten werden neue Operationsmöglichkeiten erschlossen. Über winzige Röhren werden Instrumente, Licht und Kameras in den Körper des Patienten eingeführt. Der Roboter hält die Geräte und führt die notwenigen Bewegungen aus, die der Operateur an der Konsole vorgibt. Kein Zittern, keine Kraftprobleme mehr, keine fehlende Sicht auf Operationsgebiete – denn der Roboter kann auch in Regionen arbeiten, an die das Skalpell in der Hand nicht gut hinkommt. Dabei gilt immer: Es operiert nicht das Gerät, sondern der erfahrende Chirurg, er lässt sich aber helfen, um die OP sicherer zu machen und viel mehr Möglichkeiten zu haben.
Der Da Vinci®-Roboter ist ein Assistent
Der sogenannte Telemanipulator führt keine Bewegung automatisiert oder autonom aus. Vielmehr handelt es sich um einen Computer, der die Bewegung des Chirurgen auf Mikroinstrumente überträgt. Dabei werden die Bewegungen im Verhältnis fünf zu eins auf die Instrumente übersetzt. Das heißt, fünf Zentimeter Bewegung der Hand ergibt einen Zentimeter Justierung des Instruments im Körper. Die Instrumente bewegen sich dabei absolut zitterfrei und präzise. Menschliche Schwächen werden damit ausgeschaltet, menschliche Stärken hingegen verstärkt: Denn nur, wer sowieso schon absolut sicher operiert, wird auch mit dem Da Vinci®-Gerät arbeiten. „Bei der radikalen Entfernung von Tumoren sind Genauigkeit und Präzision das oberste Ziel. Mit diesem Gerät können wir das noch besser leisten“, erläutert der Urologe.
Video-Ratgeber
DocCaro: So funktioniert eine Darmspiegelung
Die erste Folge der Videoreihe #Frag die Docs auf Youtube liefert Einblick in den menschlichen Darm. Carola Holzner alias DocCaro erklärt mit ihren Wuppertaler Kollegen Dr. Christian Giesecke und Dr. Leonard Fehring von der Klinik für Gastroenterologie, Hepatologie, Endokrinologie und Diabetologie am Helios Universitätsklinikum Wuppertal Ablauf und Nutzen einer Darmspiegelung.
Herzlich willkommen in unserem Zentrum. Hier finden Sie alle wichtigen Informationen, die Ihnen den Aufenthalt und die Behandlung bei uns so angenehm wie möglich machen.
Eine ausgewogene, auf die individuelle Situation angepasste Ernährung spielt eine große Rolle für den Heilungsprozess und das allgemeine Wohlbefinden. Für ein persönliches Gespräch stehen wir gerne nach telefonischer Vereinbarung zur Verfügung.
Eine allgemein gültige "Stomadiät" gibt es nicht!
Ernährungsempfehlungen für Menschen, die nach einer lebenserhaltenden Operation einen künstlichen Darmausgang (Stoma) tragen, entsprechen im Allgemeinen denen einer gesunden Ernährung. Die Ernährung muss aber für den Einzelnen und seine Bedürfnisse angepasst werden. Diätetische Maßnahmen nehmen Einfluss auf Stuhlkonsistenz, Windabgang und Geruchsbildung. Dennoch gibt es keine für alle Patienten verbindliche Diät.
Gesunde Ernährung ist das Ziel
Allgemein gültigen Ernährungsempfehlungen zu folgen, erscheint Stomaträgern oft zu riskant. Unsere Empfehlung ist jedoch: Prüfen Sie, tasten Sie sich heran an das, was für Sie bekömmlich und für Ihre Lebensweise mit dem Stoma zuträglich ist! Vieles, was als gesund empfohlen wird, ist sicher auch für Sie geeignet. Es gibt viele Möglichkeiten, das Essen für Sie wieder genussvoll zu machen. Zum Beispiel: Schälen Sie Obst und Gemüse öfter, zerkleinern es sorgfältiger, essen weniger davon auf einmal, wählen weniger grobe Vollkornprodukte usw. Sprechen Sie uns an, wir beraten Sie gern!
Beratung im Umgang mit dem Stoma
Wenn Sie ein Stoma (künstlicher Darm- oder Blasenausgang) bekommen, bietet Ihnen die ausgebildete Stomatherapeutin Claudia Nitschke ihre Unterstützung an. In der Zeit nach der Operation kommt sie auf die Station, um Sie aufzuklären und zu schulen. Nach telefonischer Vereinbarung steht sie bei Fragen und Problemen gerne zur Verfügung. Auch in unserem Patientenservicecenter (Haus 3a, Erdgeschoss) finden Schulungen in geeigneten Räumlichkeiten statt.
Als Darmkrebszentrum arbeiten wir eng mit der Selbsthilfegruppe Deutsche ILCO e.V. zusammen. Es gibt eine Wuppertaler Gruppe. Der Austausch mit anderen Betroffenen kann entlasten und Mut machen - eine Kontaktaufnahme ist jederzeit herzlich willkommen.
Ansprechpartnerin für die Regio Bergisch Land
Frau Gaby Forthmann, Tel. 0170-1481148, ilco-bergischland@t-online.de).
Alle Infos: www.ilco.de
Weitere Infos zu den Selbsthilfegruppen am Helios Universitätsklinikum
Ein wichtiges Qualitätskriterium für ein Krebszentrum ist die Teilnahme an klinischen Studien. Wir beteiligen uns an klinischen Studien, um neue, lebensverbessernde Therapien zu testen und frühzeitig für Patient:innen verfügbar zu machen. In unserem Darmkrebszentrum können Sie sich darauf verlassen, dass Sie nach höchsten wissenschaftlichen Maßstäben behandelt werden.
Wenn eine Studie für Sie in Frage kommt, sprechen wir eine mögliche Teilnahme mit Ihnen ausführlich und verständlich an.
42283 Wuppertal