Die TNM-Klassifikation: Wie hat sich der Tumor ausgebreitet?
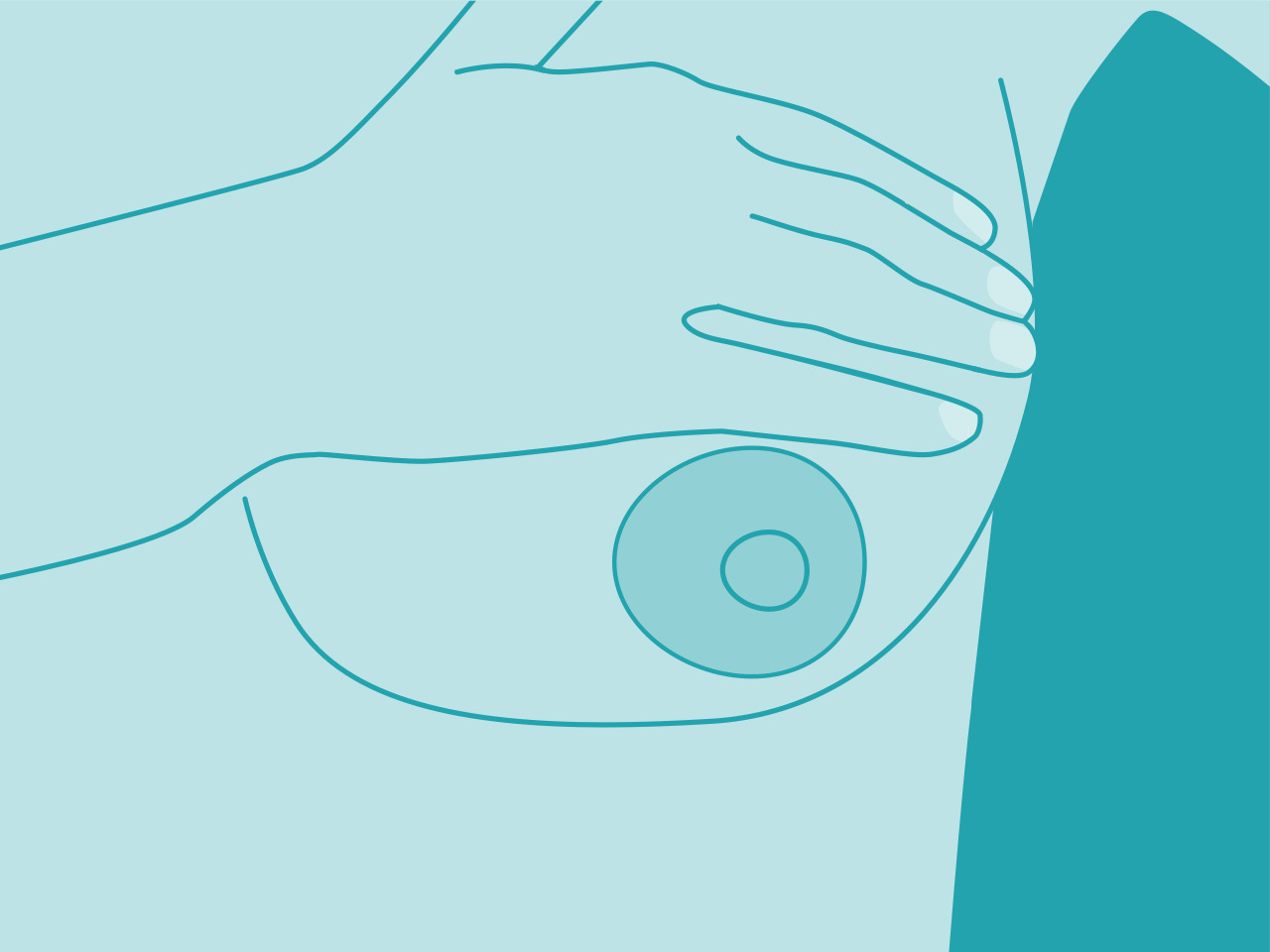
Ist der Brustkrebs diagnostiziert, stellen sich betroffene Frauen viele Fragen: Wie weit ist der Krebs fortgeschritten? Sind Lymphknoten befallen? Habe ich Metastasen?
Nicht nur für die Patientin selbst, sondern auch für den optimalen Therapieplan ist die Stadieneinteilung wichtig. International ist eine Einstufung nach drei Gesichtspunkten üblich: der sogenannten TNM-Klassifikation.
T = gibt die Größe des Tumors in Zentimetern an
N = Anzahl beziehungsweise Lokalisation der befallenen Lymphknoten (lateinisch nodi = Knoten)
M = gibt an, ob Metastasen vorhanden sind
T-Stadium:
- T0: kein Tumornachweis
- T1: der Tumor ist kleiner als 2 Zentimeter
- T2: der Tumor hat eine Größe von 2 bis 5 Zentimeter
- T3: der Tumor ist größer als 5 Zentimeter
- T4: der Tumor hat sich auf die Brustmuskulatur oder Haut ausgedehnt
N-Stadium:
- Nx: die Lymphknoten lassen sich nicht beurteilen
- N0: keine Lymphknoten befallen
- N1: Metastasen in den Lymphknoten der Achselhöhle nachweisbar
- N2: Metastasen in den Lymphknoten beider Achselhöhlen und/oder in der Nachbarschaft nachweisbar
- N3: die Lymphknoten hinter dem Brustbein sind befallen
M-Stadium:
- Mx: es kann nicht beurteilt werden, ob andere Organe Metastasen haben
- M0: kein klinischer Nachweis von Metastasen in anderen Organen
- M1: Metastasen sind in anderen Organen nachweisbar
UICC-Einteilung: In welchem Stadium befindet sich der Brustkrebs?
Neben der TNM-Klassifikation nutzt man beim Mammakarzinom zusätzlich die Einteilung der zur Weltgesundheitsorganisation gehörenden UICC (französisch: Union internationale contre le cancer). Diese fasst die TNM-Einstufungen zu Stadien zusammen [1].
Brustkrebs Stadium 0
Im UICC Stadium 0 liegt ein duktales oder lobuläres Carzinoma in situ (Tis) vor, sprich: eine Krebsvorstufe. Es sind keine Lymphknoten betroffen (N0) und es gibt keine Metastasen (M0).
Brustkrebs Stadium I
Im UICC Stadium IA liegt ein Tumor vor, der kleiner als zwei Zentimeter ist (T1). Es sind keine Lymphknoten betroffen (N0) und es gibt keine Fernmetastasen (M0).
Im UICC Stadium IB gibt es keinen Tumor (T0) oder einen Tumor von nicht mehr als zwei Zentimeter Größe (T1); in den Lymphknoten konnten Mikrometastasen zwischen 0,2 bis 2 Millimeter Durchmesser nachgewiesen werden (N1mic), jedoch gibt es keine Fernmetastasen (M0).
Brustkrebs Stadium II
Im UICC Stadium IIA gibt es keinen Tumor (T0) oder einen Tumor von nicht mehr als zwei Zentimeter Größe (T1); in den Lymphknoten konnten wenige Metastasen nachgewiesen werden (N1), jedoch gibt es keine Fernmetastasen (M0).
Vom Stadium IIA wird auch gesprochen, wenn der Tumor zwischen zwei und fünf Zentimetern groß ist (T2), jedoch weder Lymphknoten (N0) befallen sind noch Fernmetastasen (M0) vorliegen.
Im UICC Stadium IIB ist der Tumor zwischen zwei und fünf Zentimetern groß (T2), es sind wenige Lymphknoten befallen (N1) und es liegen keine Metastasen in anderen Organen vor (M0). Zudem wird vom Stadium IIB gesprochen, wenn der Tumor größer als 5 Zentimeter ist (T3), jedoch weder die Lymphknoten befallen sind (N0) noch Fernmetastasen (M0) vorliegen.
Brustkrebs Stadium III
Im UICC Stadium IIIA gibt es keinen Tumor (T0) oder einen Tumor bis fünf Zentimeter Größe (T1 oder T2), es sind Metastasen in den Lymphknoten beider Achselhöhlen oder in der Nachbarschaft nachweisbar (N2), jedoch keine Fernmetastasen (M0)
Außerdem wird vom Stadium IIIA gesprochen, wenn der Tumor größer als 5 Zentimeter ist (T3), Krebszellen in den Lymphnoten einer Achselhöhle (N1) oder in den Lymphknoten beider Achselhöhlen (N2) nachweisbar sind, jedoch keine Fernmetastasen vorliegen (M0).
Im UICC-Stadium IIIB hat der Tumor sich auf die Brustmuskulatur oder Haut ausgedehnt, die Lymphknoten sind entweder gar nicht befallen (N0), es ist nur eine Achselhöhle befallen (N1) oder beide (N2), jedoch liegen keine Fernmetastasen vor (M0).
Im UICC-Stadium IIIC sind unabhängig von der Tumorgröße (jedes T) die Lymphknoten auch hinter dem Brustbein befallen (N3), es liegen jedoch keine Fernmetastasen vor (M0).
Brustkrebs Stadium IV
Im UICC-Stadium IV sind Fernmetastasen vorhanden (M1), unabhängig von der Größe des Tumors (jedes T) oder einem Lymphknotenbefall (jedes N).
Die UICC-Stadien 0 und I werden als frühe Stadien bezeichnet, die Stadien II und III als fortgeschrittene Stadien und das Stadium IV als metastasiertes Stadium.
Folgendes Diagramm zeigt die Verteilung der UICC Stadien bei Erstdiagnosen (Jahre 2015-2016) [2]:
Was ist ein Tumormarker bei Brustkrebs?
Tumormarker sind Substanzen, die entweder von Tumorzellen selbst gebildet werden, beispielsweise als Stoffwechselprodukte, oder die von gesunden Zellen als Reaktion auf das Vorliegen von Tumorzellen produziert werden. Meist wird über eine Blutprobe geprüft, ob Tumormarker vorhanden sind, zum Teil liegen sie jedoch auch in anderen Körperflüssigkeiten vor. Tumormarker können einerseits prädektiv sein, sprich etwas über den Erfolg einer bestimmten Therapie aussagen, oder als Prognosefaktor genutzt werden, also Informationen über den wahrscheinlichen Krankheitsverlauf geben.
Die wichtigsten Tumormarker bei einem Mammakarzinom sind:
- CA 15-3
- CEA (karzinoembryonales Antigen)
Welche Werte sind normal?
Der Marker CA15-3 ist ein typischer Tumormarker für Brustkrebs. Er wird über das Blut bestimmt, der Normalwert liegt bei unter 28 Units pro Milliliter Blut.
Der Marker CEA ist ein relativ unspezifischer Tumormarker, der neben Brustkrebs auch auf Krebserkrankungen der Lunge, des Magens oder Dickdarms hinweisen kann. Der Normalwert liegt bei bis zu fünf Mikrogramm pro Milliliter Blut.
Brusterhaltende Operation: Wann wird sie angewandt?
Bei einer Brustkrebserkrankung steht unter anderem die operative Therapie zur Verfügung. Heute nutzen die behandelnden Ärzte, wann immer möglich, brusterhaltende Verfahren. Voraussetzung für brusterhaltendes Operieren ist die Möglichkeit, dabei den gesamten Tumor entfernen zu können.
Lage und Größe der Geschwulst sowie das Größenverhältnis von Tumor und Brust spielen dabei eine große Rolle: Ist das Karzinom einzeln und örtlich begrenzt, kann die Brust in der Regel erhalten werden.
Eine andere Möglichkeit ist eine Kombination aus Chemotherapie und brusterhaltender Operation: Vor der Operation wird eine Chemotherapie („neoadjuvante Chemotherapie“) oder Antikörpertherapie durchgeführt, die den bösartigen Tumor soweit verkleinert, dass er anschließend brusterhaltend entfernt werden kann.
Ablauf der Operation
Im Rahmen der Operation werden der Tumor und seine Umgebung sowie einige Lymphknoten der Achselhöhle entfernt. Je nach Ausbreitung und Lage der Krebszellen sind unterschiedliche Operationen möglich:
Knotenentfernung: Unter Narkose oder nach örtlicher Betäubung wird die Haut über dem Tumor durchtrennt. Der Knoten wird mit einem Sicherheitsabstand entfernt und so markiert, dass der Pathologe genau weiß, wie der Befund in der Brust gelegen hat. Der Gewebedefekt ist meist klein und bedarf selten einer plastischen Rekonstruktion. Betroffene Frauen sehen in der Regel nicht, dass Gewebe in der Brust fehlt. Das Verfahren eignet sich nur bei einem kleinen Tumor und günstigem Größenverhältnis zur Brust.
Teilentfernung des Brustdrüsengewebes: Die Methode ist ähnlich der Knotenentfernung, nur wird wesentlich mehr Gewebe aus der Brust entfernt. Die Muskelhaut unter dem Tumor wird dabei immer mit weggenommen. Gelegentlich wird auch etwas Haut über dem Tumor entfernt. Der Gewebedefekt ist umfangreicher und häufig ist eine Formrekonstruktion der Brust nötig.
In Abhängigkeit von der Brustgröße kann Eigengewebe aus der operierten Brust zum Defektausgleich genutzt werden. Da eine bestimmte Gewebemenge aus der kranken Brust entfernt wird, kommt es häufig zum Größenunterschied zur gesunden Brust. Dieser kann durch eine Verkleinerung der gesunden Seite ausgeglichen werden.
Eine Verkleinerung der Brust kann manchmal zum Vorteil der Therapie sein. Große Brüste können schlechter nachbestrahlt werden, die Komplikationsraten sind im Allgemeinen recht hoch. Oft ist diese Technik ein doppelter Gewinn für die Patienten. Nicht nur der Krebs ist operiert, eine häufig störende Übergröße der Brust, mit Nacken- und Rückenschmerzen, wird gleich mitbehandelt.
Komplette Ausschälung des Drüsengewebes: Mit einem elektrischen Messer, einer Schere oder einem Skalpell gelingt es, die Brustdrüse komplett aus der Haut herauszulösen. Der Gewebeausgleich erfolgt über Implantate oder Eigengewebe von unterschiedlichen Körperregionen. Eine Bestrahlung von Brustprothesen nach einer Operation sollte wegen des Fibroserisikos vermieden werden. Alternativ kann bis zum endgültigen Wiederaufbau ein sogenanntes Platzhalterimplantat vor der Bestrahlung eingesetzt werden.
Mitentfernung der Brustwarze: Alle Milchkanäle laufen auf der Brustwarze zusammen. Liegt eine Krebserkrankung vor, deren Ursprung in den Milchkanälen liegt, kann eine Operation der Brustwarze nötig sein. Manchmal können wir während der Operation nicht genau sehen, ob hier eine Krebserkrankung vorliegt. Je nach Befund durch die Pathologie, muss in einer zweiten, kleineren Operation die Brustwarze entfernt werden.
Radikale Brust-Operation (Brustamputation)
Bei ungefähr 30 Prozent der an Brustkrebs erkrankten Frauen ist es unumgänglich, die Brust zu entfernen – auch Mastektomie genannt. Diese radikale Methode dient der Sicherheit der Patientinnen, nicht wieder zu erkranken.
Verständlicherweise haben die meisten Frauen nach einer Brustamputation den Wunsch, die fehlende Brust so schnell und gut wie möglich zu ersetzen. Die Möglichkeiten reichen von einer BH-Prothese bis hin zur vollständigen Neubildung einer Brust durch Implantate oder Eigengewebe.
Manchmal wünschen sich Brustkrebspatientinnen auch die Brustentfernung, um eine Bestrahlung zu vermeiden. Insbesondere ältere Frauen können mitunter durch eine radikale Brust-Operation schonender behandelt werden.
Was passiert im Körper bei der Brustamputation?
Wenn die Brust entfernt wurde, findet die Patientin eine feine, etwas schräg verlaufende Narbe auf der Brustwand. In einigen Fällen gelingt es, den in der Mitte liegenden Anteil der Brust zu erhalten und so ein schönes Dekolleté zu schaffen. Die seitlichen Bereiche der Brust werden dann mit einem Silikonkissen, das im BH liegt oder auf der Haut klebt, ausgeglichen.
Lymphknoten-Entfernung
Diese Maßnahme ist ein immer notwendiger Teil der Brustoperation bei einem Mammakarzinom.
Wie in einem Kanalisationssystem werden die Tumorzellen von den Lymphknoten gefiltert. Wird nur der Knoten aus der Brust entnommen, während die krankhaften Zellen in den Lymphknoten verbleiben, kann das nachteilig für die Heilung sein. Deshalb ist es wichtig zu wissen, ob die Lymphknoten befallen sind. Hierzu gibt es unterschiedliche Verfahren: die klassische Entfernung von mindestens zehn Lymphknoten oder die Entfernung weniger Wächterlymphknoten, die Informationen darüber geben, ob die Achselhöhle Tumorzellen enthält.
Klassische radikale Entfernung
Bei der klassischen Technik wird von der Operationswunde auf der Brust oder von einem separaten Schnitt in der Achselhöhle aus Lymphknotenfettgewebe entfernt. Im Bereich der Achselhöhle liegen zahlreiche Nerven und Gefäße auf sehr engem Raum beieinander. Die klassische ausgedehntere Entfernung der Lymphknoten ist daher mit Nebenwirkungen verbunden, die viele Patientinnen als nachteilig empfinden.
Eine Bewegungseinschränkung des Schultergürtels, ein vorübergehendes Taubheitsgefühl auf der Innenseite des Oberarms, Narbenzüge in der Achselhöhle, eine Zunahme des Armumfanges (Lymphödem) werden zum Teil noch Jahre später angegeben. Etwa die Hälfte aller Patientinnen ist nach der klassischen Lymphknotenentfernung von Nebenwirkungen betroffen.
Präparation des Wächterlymphknotens (Senitel Node)
Diese sehr schonende Methode der Lymphknotenentfernung arbeitet mit einer sehr schwachen radioaktiven Markierung, die das betroffene Gewebe präzise darstellt. Es gibt bestimmte Kriterien, wann das Verfahren genutzt werden kann. Die Behandlung bedarf der längeren Erfahrung des Operateurs und einer guten Zusammenarbeit mit den Ärzten für Nuklearmedizin, die für den Operateur die radioaktiv markierte Substanz spritzen.
Pathologische Aufarbeitung – Stadieneinteilung – Prognosefaktoren
Die entnommenen Lymphknoten werden, genau wie der Knoten und das mitgenommene umliegende Gewebe, vom Pathologen sorgfältig untersucht. Die Wächterlymphknoten erhalten nach der lichtmikroskopischen Untersuchung eine Spezialfärbung, um kleinste Zellreste aufspüren zu können. Die Arbeit des Pathologen ist ein wichtiger Baustein in der Brustkrebsbehandlung. Er bestimmt die Tumorart, ob im Gesunden operiert wurde und vieles mehr. Es liegt auch in seiner Hand, biochemische Untersuchungen auf der Oberfläche der Tumorzellen durchzuführen. Hierbei wird u.a. erkannt, ob ein Tumor auf Hormone sensibel ist. Der Status der Lymphknoten ist ein wesentliches Kriterium zur Stadieneinteilung der Erkrankung. Das Stadium ist wiederum zwingend für die Diskussion der Fachärzte in der Tumorkonferenz, in der die Gesamttherapie geplant wird.
Chemotherapie bei Brustkrebs
Bei der Behandlung von Brustkrebserkrankungen kommt der medikamentösen Therapie neben der Chirurgie und der Strahlentherapie eine besondere Bedeutung zu.
Eine Chemotherapie ist bei der Diagnose Brustkrebs nicht immer der einzige Weg: Dr. Christoph Großmann, Ärztlicher Leiter des Brustzentrums der Helios Mariahilf Klinik Hamburg, erklärt, was es zu beachten gibt bei der Frage: Chemo - ja oder nein?
Wann wird die Chemotherapie angewandt?
Die Chemotherapie kann vor einer Operation zum Einsatz kommen, um den Tumor zu verkleinern und so das spätere Operationsergebnis zu verbessern. Mediziner bezeichnen diese Behandlung als neoadjuvante Chemotherapie. Sie kann aber auch nach einer Operation nötig werden. Diese als adjuvante Chemotherapie bezeichnete Anwendung wird vor allem eingesetzt, um ein erhöhtes Metastasierungsrisiko zu senken.
Was passiert im Körper bei einer Chemotherapie?
Da sich Tumorzellen sehr schnell teilen und sich im Falle einer Zerstörung nur schwer wieder reparieren lassen, setzt die Chemotherapie auf Medikamente (Zytostatika), die direkt auf das Wachstum von Tumorzellen wirken. Dadurch kann in vielen Fällen eine deutliche Verkleinerung, im besten Fall sogar eine komplette Rückbildung der Tumorzellen erreicht werden.
Ablauf der Therapie
Bei der Chemotherapie werden verschiedene Substanzen miteinander kombiniert. Ein Therapie-Schema legt vorab fest, wann der Patientin wie viel von welchem Medikament verabreicht wird. Die normalerweise im Abstand von drei bis vier Wochen stattfindenden Anwendungen sollten von einem auf Chemotherapie spezialisierten Arzt durchgeführt werden.
Patientinnen mit einem metastasierten Tumor erhalten eine auf ihren Allgemeinzustand und die Wachstums- und Metastasierungsgeschwindigkeit des Tumors abgestimmte Therapie, die sowohl als Einzeltherapie (Monochemotherapie) als auch als Kombination (Polychemotherapie) gegeben werden kann.
Heutzutage stehen auch neuartige Medikamente wie zielgerichtete Antikörper oder Immuntherapeutika auch in Kombination mit einer antihormonellen Therapie für den Einsatz bei metastasierten Brustkrebserkrankungen zur Verfügung. So konnte die Prognose, aber auch die Verträglichkeit und Lebensqualität für die Patientinnen gesteigert werden.
Welche Nebenwirkungen gibt es?
Die Chemotherapie greift nicht nur schnell wachsende Krebszellen an, sondern wirkt sich auch auf gesunde, sich schnell teilende Zellen des Körpers, wie etwa Haarwurzelzellen, Zellen des Magen-Darm-Trakts und Geschlechtszellen aus: Haarausfall sowie Übelkeit und Erbrechen können daher auftreten.
Auch vermindert eine Chemotherapie unter Umständen die Anzahl an weißen und roten Blutkörperchen im Blut, sodass der Körper gegenüber Infektionen anfälliger wird und das Blutungsrisiko sowie das Risiko einer Blutarmut (Anämie) steigen.
Durch die Einführung zahlreicher Medikamente, die die früher oft gefürchteten Nebenwirkungen der Chemotherapie reduzieren, ist es möglich geworden, fast alle gängigen Chemotherapien auch ambulant zu verabreichen. Den Patientinnen wird somit ein längerer Klinikaufenthalt erspart. In der Regel übernehmen die Krankenkassen die Kosten für ein Taxi zur und von der Onkologischen Praxis.
Hormonbehandlung: Wann wird sie angewandt?
Eine Hormonbehandlung kommt insbesondere für Frauen mit hormonell empfindlichen Brustkrebszellen infrage: Progesteron und Östrogen, zwei körpereigene weibliche Geschlechtshormone, können den Brustkrebs zum Wachsen anregen. Im Labortest wird zunächst ermittelt, ob die Tumorzellen Hormonrezeptoren (Link Brustkrebs Übersicht > Hormonrezeptoren) aufweisen und somit zum Wachsen angeregt werden. Ist dies der Fall, kann eine antihormonelle Therapie durchgeführt werden. Dafür steht eine Reihe von Medikamenten zur Verfügung, deren Wirkstoffe unterschiedliche Angriffspunkte haben.
Ablauf der Therapie
Üblicherweise erfolgt nach der Operation über fünf bis zehn Jahre eine Behandlung mit dem Antiöstrogen Tamoxifen im Wechsel mit einem Aromatasehemmer. Bei Frauen vor den Wechseljahren können Medikamente verabreicht werden, die die Eierstockfunktion unterbrechen, sogenannte GnRH-Analoga.
Durch Aromatasehemmer kann eine Osteoporose verstärkt werden. Eine Knochendichtemessung kann in Einzelfällen Klarheit verschaffen. Gegen Osteoporose werden vorsorglich knochenschützende Medikamente eingesetzt, die Osteoprotektiva.
Welche Nebenwirkungen gibt es?
Die bei der Hormontherapie auftretenden Beschwerden ähneln einigen Wechseljahresymptomen: Hitzewallungen, Übelkeit und wechselhafte Stimmungen können die Folgen einer solchen Therapie sein. Manche Wirkstoffe können auch zu einem Nachlassen der sexuellen Lust oder zur Gewichtszunahme durch Wassereinlagerungen führen.
Wann wird die Strahlentherapie angewandt?
Eine weitere Säule bei der Behandlung des Brustkrebses ist die Strahlentherapie. Sie kommt im Allgemeinen dann zum Einsatz, wenn bei der Operation die Brust erhalten werden konnte beziehungsweise wenn Lymphknoten befallen sind.
Video-Interview mit Prof. Dr. med. Marc. Piroth, Chefarzt der Klinik für Strahlentherapie und Radio-Onkologie im Helios Universitätsklinikum Wuppertal.
Ablauf der Therapie
Ähnlich wie bei der Chemotherapie wird auch bei der Strahlentherapie bewusst das Erbgut entarteter Zellen irreparabel geschädigt. Anders als gesunde Zellen sind Tumorzellen nicht in der Lage, die durch die Bestrahlung hervorgerufenen Schäden am Zellkern zu reparieren, sodass Tumorzellen letztendlich vernichtet und ein erneutes Wachstum von Tumoren verhindert werden. In der Regel beginnt der Arzt drei Wochen nach der Operation bzw. im Anschluss an die Chemotherapie mit der Behandlung; diese dauert etwa fünf bis sechs Wochen. In dieser Zeit wird die Patientin wöchentlich fünfmal für einige Minuten mit einer niedrigen Strahlendosis behandelt. Die Aufteilung der Bestrahlungseinheiten in diese vielen kleinen Einzeldosen erhöht nochmals die Verträglichkeit.
Welche Nebenwirkungen gibt es?
Bei der Strahlentherapie wird immer auch ein Teil der Lunge mitbestrahlt. Die Folge kann eventuell eine Art Lungenentzündung sein. Wenn die Tumorzellen mit Röntgenstrahlen erreicht werden, können auch gesunde Hautzellen in Mitleidenschaft geraten. Daher kann es zu Hautrötungen und -reizungen (ähnlich wie bei einem Sonnenbrand) kommen. Bei vielen Patientinnen kann auch verstärkt Müdigkeit und Abgeschlagenheit auftreten, vor allem gegen Ende der Behandlung.
Immuntherapie: Wann wird sie angewandt?
Man muss eine Antikörpertherapie gegen gezielte Rezeptoren mit Wirkstoffen wie Trastuzumab, Pertuzumab oder TDM-1 von einer Immuntherapie gegen sogenannte T-Zell-Checkpoint-Inhibitoren oder gegen den PD-L1 Rezeptor mit Wirkstoffen wie Pembrolizumab, Tezolizumab oder Durvalumab unterscheiden.
Bei circa 20 Prozent der bösartigen Brusttumore kommt es zu einer vermehrten Bildung bestimmter Wachstumsfaktoren (c-erb2) und des Wachstumsfaktor-Rezeptors (HER-2, human epidermaler Wachstumsfaktor-Rezeptor 2). Diese senden pausenlos das Signal „Bitte wachsen!“ an die Zellkerne der Tumorzellen. Die Folge: Das Krebsgeschwür breitet sich rasant und unkontrolliert aus.
Die Immuntherapie ist hier – meist in Kombination mit einer Chemotherapie – der Therapieansatz: Durch die Gabe von Antikörpern kann die Signalweiterleitung blockiert und der Tumor am Wachsen gehindert werden. Im besten Fall sterben die Tumorzellen ab (Apoptose) und der Tumor verkleinert sich.
Ablauf der Therapie
Solche Antikörper bei Brustkrebs sind Trastuzumab beziehungsweise Pertuzumab. Die Substanz dockt sich an den Wachstumsfaktor-Rezeptor an und unterbindet die wachstumsfördernde Wirkung. Der Brustkrebs wird in seinem Wachstum gehemmt. Die Verabreichung erfolgt als Infusion durch die Vene (intravenös). Die Behandlung dauert in der Regel zwei Stunden. Ebenso zugelassen ist auch das Antikörper-Zytostatikum- Konjugat TDM-1, das bei Frauen verabreicht wird, deren Tumor nach der neoadjuvanten Behandlung nicht durch einen kompletten Rückgang (Remission) reagiert hat.
Welche Nebenwirkungen gibt es?
Da die Immuntherapie auf eine Aktivierung des körpereigenen Abwehrsystems setzt, kann sie zu grippeähnlichen Symptomen führen. Dies wird jedoch sehr selten und auch nur am Anfang der Infusionsbehandlung beobachtet.
Die Therapie von metastasiertem Brustkrebs
Haben sich die Krebszellen vom Zellverbund gelöst und sind in ferne Organe eingedrungen, spricht man von metastasiertem Brustkrebs. Durch die Therapie eine vollständige Entfernung der Krebszellen aus dem Körper und damit eine Heilung zu erreichen, gilt dann als unwahrscheinlich. Die Erkrankung wird als chronisch bezeichnet.
Je nachdem, in welchem Organ sich die Metastasen befinden, ist der Krankheitsverlauf unterschiedlich. Bei Patientinnen mit Tochtergeschwulsten in Haut und Knochen kann die Erkrankung mit den heutigen medizinischen Möglichkeiten oft über Jahre gut kontrolliert werden. Frauen mit Metastasen in Lunge, Leber und Gehirn haben eine schlechtere Prognose.
Wie bei der Therapie von frühem und fortgeschrittenem Brustkrebs, wird auch bei metastasiertem Brustkrebs eine Behandlung mit Chemotherapie, Antihormoneller Therapie oder Immuntherapie beziehungsweise einer Kombination dieser Verfahren vorgeschlagen (systemische Therapie).
Zudem kann auch hier, je nach Lage aus Ausbreitung der Metastasen, als lokale Therapie eine Bestrahlung oder Operation sinnvoll sein.
Die palliative Behandlung
Der Begriff „palliativ“ stammt aus dem Lateinischen und bezieht sich auf „Pallium“, was so viel wie „Mantel“ oder auch „bewahren“ bedeutet. Die Palliativversorgung soll den Menschen also wie einen Mantel umhüllen und Schutz geben. Damit sind Therapieoptionen für unheilbar an Krebs erkrankte Menschen gemeint. Ziel dieser Therapie ist es, die Patientin in die Lage zu versetzen, solange wie möglich, mit so guter Lebensqualität wie möglich und so beschwerdearm wie möglich zu leben.
Was bedeutet Palliativmedizin und was sind palliative Therapien?
Wird ein Mammakarzinom als nicht heilbar eingestuft, so wird die Behandlung als „palliativ“ bezeichnet. Hierbei unterscheidet man zwischen der Palliativmedizin und den palliativen Therapien.
Die Palliativmedizin ist ein Ansatz zur Verbesserung der Lebensqualität von Patientinnen und ihren Familien, die mit den Problemen konfrontiert sind, die mit lebensbedrohlichen Erkrankungen einhergehen. Ihr Ziel ist es, Leiden vorzubeugen und zu lindern. Dafür ist es wichtig, Schmerzen sowie anderen belastenden Beschwerden körperlicher, psychosozialer und spiritueller Art (Definition Palliative Care WHO 2002) frühzeitig zu erkennen und sorgfältig einzuschätzen und zu behandeln.
Palliative Therapien sind gegen die Grunderkrankung gerichtet. Hierbei werden medikamentöse und nicht-medikamentöse Maßnahmen eingesetzt, um das Leben zu verlängern und/oder die Symptome zu kontrollieren. Dazu gehören zum Beispiel Chemo-und Strahlentherapien aber auch Operationen zur Symptomlinderung und Tumorverkleinerung.
Bei einer nichtheilbaren Brustkrebserkrankung ist es für die Patientinnen hilfreich, frühzeitig Konzepte der Palliativmedizin in das Behandlungskonzept mit einzubeziehen. Abhängig von dem Wunsch der Betroffenen und ihrem Allgemeinzustand sollten gleichzeitig palliative Therapien angeboten worden.
Wann ist es sinnvoll, palliative Therapien durchzuführen?
Symptomorientierte Maßnahmen können alleine oder gleichzeitig mit tumorbezogenen oder ursächlichen Therapien durchgeführt werden. Bei der Entscheidung zu einer palliativen Therapie, wie zum Beispiel einer Chemotherapie mit dem Ziel einer Symptomlinderung und Lebensqualitätsverbesserung, sind vor allem der Allgemeinzustand und die Begleiterkrankungen der Patientinnen entscheidend. Da Palliativpatientinnen oft bereits durch den Tumor und die Metastasen entkräftet sind, müssen für jede weitere Behandlung Risiko und Nutzen gut abgewogen werden. Mögliche Nebenwirkungen einer palliativen Chemotherapie sind Schwäche, Übelkeit, Erbrechen, Haarausfall oder chronische Müdigkeit. Ebenso kann ein operativer Eingriff mit entsprechender Narkose eine große Belastung für den geschwächten Organismus der Patientinnen sein.
Welche Hilfe kann die Palliativmedizin Brustkrebspatientinnen bieten?
Besonders ausgeprägte Fähigkeiten der Palliativmedizin liegen:
- in der Einschätzung und Behandlung von physischen, psychischen und spirituellen Symptomen sowie der Linderung von Leid
- in der klinischen Auseinandersetzung und Entscheidungsfindung in schwierigen Situationen, wie zum Beispiel bei der Abwägung von Bedürfnissen, Einstellungen und Belangen des Patienten
- in der Kommunikation und in der Versorgungskoordination
- in der Zusammenarbeit mit Partnern, Kollegen und Organisationen, um den Patienten und ihren Nahestehenden eine hochwertig multiprofessionelle Versorgung zur Verfügung zu stellen
- in der Unterstützung der Nahestehenden, einschließlich der Angebote zur Trauerarbeit